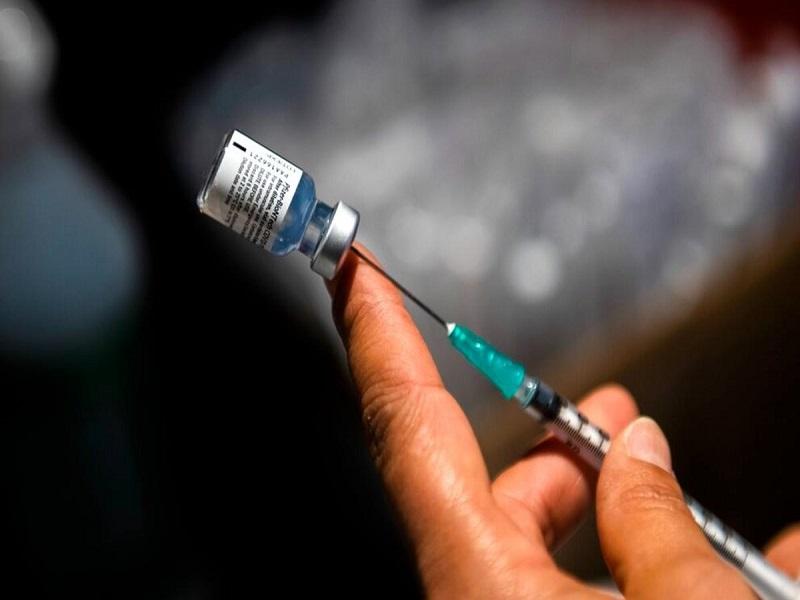
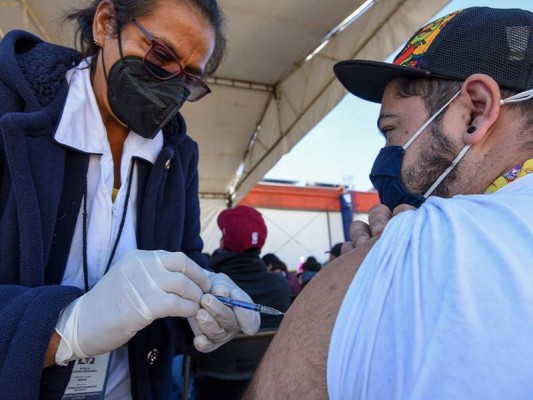
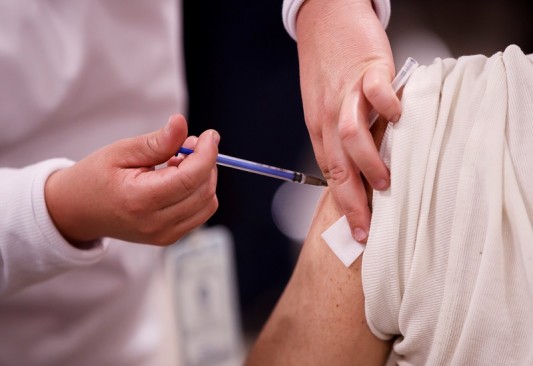
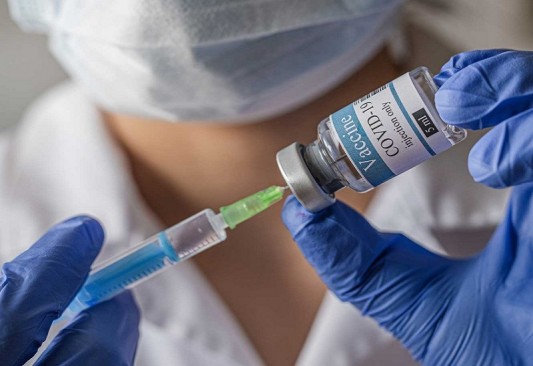
Los refuerzos de la vacuna covid-19 pueden comenzar para algunos adultos estadounidenses
Después de días de largo debate entre los expertos en vacunas, las vacunas de refuerzo de la vacuna Pfizer / BioNTech Covid-19 ahora se pueden administrar oficialmente a algunos adultos en los Estados Unidos.
La madrugada del viernes, la directora de los Centros para el Control y la Prevención de Enfermedades de los Estados Unidos, la dra. Rochelle Walensky, se separó de los asesores independientes de vacunas de la agencia para recomendar refuerzos para un grupo más amplio de personas, aquellas de 18 a 64 años que tienen un mayor riesgo de Covid-19 debido a sus lugares de trabajo o entornos institucionales, además de adultos mayores, residentes de centros de atención a largo plazo y algunas personas con afecciones de salud subyacentes.
La recomendación de los CDC incluye las recomendaciones hechas por su Comité Asesor sobre Prácticas de Inmunización el jueves, cuando votó para recomendar refuerzos para personas de 65 años o más y residentes de centros de atención a largo plazo que recibieron la serie de vacunas Pfizer / BioNTech Covid-19 hace al menos 6 meses, y personas de 50 a 64 años con afecciones médicas subyacentes.
Los CDC también respaldaron la recomendación de los asesores de vacunas de que las personas de 18 a 49 años con afecciones médicas subyacentes puedan recibir un refuerzo en función de sus beneficios y riesgos individuales.
Sin embargo, los miembros del ACIP votaron 9-6 en contra de recomendar refuerzos para las personas de 18 a 64 años que estaban en mayor riesgo debido a sus entornos ocupacionales o institucionales, como los trabajadores de la salud, los cuidadores de personas frágiles o inmunocomprometidas, personas en refugios para personas sin hogar y personas en centros correccionales.
La recomendación de Walensky se alineó con la Administración de Alimentos y Medicamentos de los Estados Unidos; el miércoles, dio autorización de uso de emergencia para una dosis de refuerzo de la vacuna Covid-19 de Pfizer en personas de 65 años o más, personas con alto riesgo de enfermedad grave y personas cuyos trabajos los ponen en riesgo de infección.
Como Director de los CDC, es mi trabajo reconocer dónde nuestras acciones pueden tener el mayor impacto. En los CDC, tenemos la tarea de analizar datos complejos, a menudo imperfectos, para hacer recomendaciones concretas que optimicen la salud. En una pandemia, incluso con incertidumbre, debemos tomar medidas que anticipamos que harán el mayor bien, dijo Walensky en el comunicado.
Creo que podemos atender mejor las necesidades de salud pública de la nación al proporcionar dosis de refuerzo para los ancianos, los que están en centros de atención a largo plazo, las personas con afecciones médicas subyacentes y los adultos con alto riesgo de enfermedad por exposiciones ocupacionales e institucionales a COVID-19. Esto se alinea con la autorización de refuerzo de la FDA y hace que estos grupos sean elegibles para una vacuna de refuerzo. Hoy, el ACIP solo revisó los datos de la vacuna de Pfizer-BioNTech. Abordaremos, con el mismo sentido de urgencia, las recomendaciones para las vacunas de Moderna y J&J tan pronto como esos datos estén disponibles.
Los debates sobre los refuerzos aumentaron en agosto cuando los funcionarios de salud de Estados Unidos anunciaron que Estados Unidos los ofrecería a las personas que habían recibido vacunas de ARNm unos ocho meses antes, a la espera de la aprobación de la FDA y los CDC. Sin embargo, los datos sobre la seguridad y eficacia de las dosis de refuerzo fueron limitados.
Pfizer había pedido a la FDA la aprobación completa de una dosis de refuerzo para todas las personas mayores de 16 años seis meses después de que fueron completamente inmunizados con dos inyecciones. La compañía argumentó que tenía suficiente evidencia de que la inmunidad comienza a disminuir después de seis meses y que dar un refuerzo restaura la inmunidad de manera segura.
Se están generando más datos sobre las dosis de refuerzo en los Estados Unidos e Israel, en particular, y la elegibilidad para los refuerzos puede abrirse en el futuro.
Moderna ha pedido a la FDA que autorice las vacunas de refuerzo para su vacuna, pero la FDA hasta ahora solo ha considerado la oferta de Pfizer. Johnson & Johnson publicó datos parciales esta semana que, según dijo, mostraron que una dosis de refuerzo elevó en gran medida la inmunidad, pero la compañía aún no ha solicitado con la FDA considerar una dosis de vacuna de refuerzo.
Con información de CNN
Compartir nota