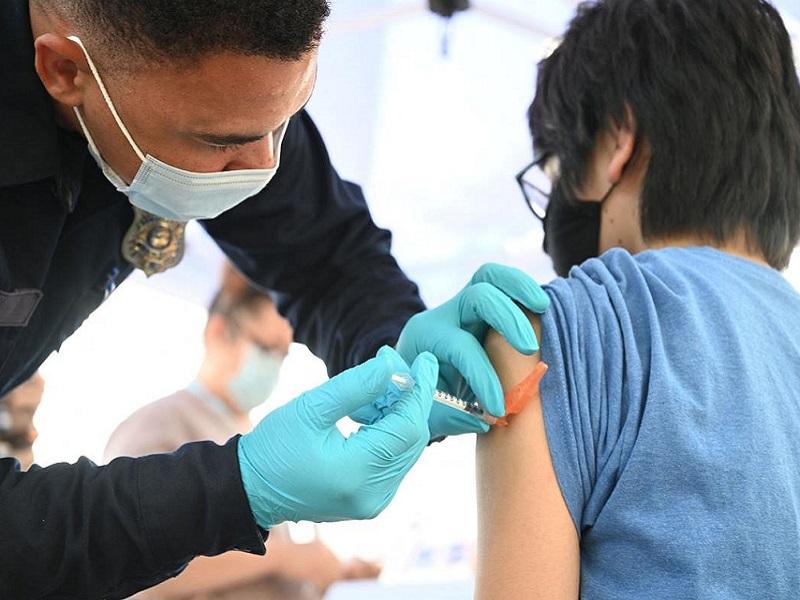
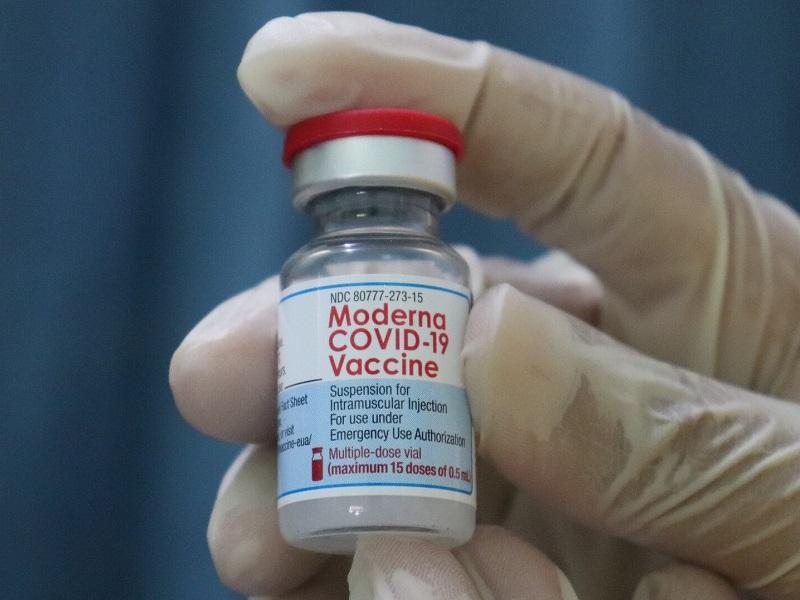
EU autoriza tercera dosis antiCovid de Pfizer para mayores de 65 años y de alto riesgo
La Administración de Alimentos y Medicamentos (FDA, en inglés) autorizó este miércoles por la noche una tercera dosis de refuerzo de Pfizer para personas mayores de 65 años o aquellas que corren un alto riesgo.
El anuncio se produjo días después de que un grupo asesor de la FDA rechazara abrumadoramente un plan generalizado de la Casa Blanca para aplicar un tercer refuerzo de la vacuna a la población que ya ha recibido dos dosis. En cambio, ese panel respaldó las dosis de refuerzo de la vacuna Pfizer solo para las personas de 65 años o mayores y las personas con alto riesgo de contraer el virus.
Si bien las vacunas contra covid-19 continúan ofreciendo una fuerte protección contra enfermedades graves, hospitalización y muerte, la inmunidad contra infecciones más leves parece estar disminuyendo meses después de la vacunación, aunque las investigaciones no han sido del todo concluyentes.
Este miércoles, un influyente panel de asesores de los Centros para el Control y la Prevención de Enfermedades abordó la cuestión sobre qué estadounidenses deberían recibir inyecciones de refuerzo de covid-19, y algunos miembros se preguntaron si la decisión debería posponerse un mes con la esperanza de obtener más evidencia.
Las dudas e incertidumbres sugirieron alrededor de si aplicar dosis adicionales para apuntalar la protección de los estadounidenses contra el coronavirus es científicamente más complicada de lo que la administración Biden pudo haberse dado cuenta cuando describió los planes hace un mes para una estrategia generalizada. Se suponía que el lanzamiento había comenzado esta semana.
Gran parte de la discusión en la reunión del Comité Asesor de Prácticas de Inmunización de los CDC se centró en la posibilidad de un programa de refuerzo reducido dirigido a las personas mayores o quizás a los trabajadores de la salud. Pero incluso entonces, algunos de los expertos dijeron que no estaban claros los datos sobre si realmente se necesitan refuerzos, quién debería recibirlos y cuándo.
Hacia el final de la reunión, el comité dijo que esperarán escuchar más de la FDA antes de seguir discutiendo la necesidad de refuerzos de la vacuna. Un posible segundo día de discusiones está programado para el jueves.
Si hay una autorización de la FDA para el mediodía de mañana, celebraremos la reunión según lo programado, dijo en la reunión la doctora Amanda Cohn, asesora principal de vacunas de los CDC y secretaria ejecutiva de ACIP. De lo contrario, la reunión del jueves podría reprogramarse, comentó.
Con información de Univisión